Obtenez votre Devis Gratuit
Le lipœdème est une pathologie quasi exclusivement féminine, dont les poussées évolutives coïncident invariablement avec les grandes transitions hormonales de la vie reproductive. Ce constat clinique pointe vers les œstrogènes comme acteurs centraux de sa physiopathologie. Cet article analyse les preuves biologiques, histologiques et épidémiologiques qui soutiennent le rôle des œstrogènes dans le déclenchement et la progression du lipœdème, explore les mécanismes moléculaires impliqués, discute les nuances du lien de causalité, et présente les perspectives thérapeutiques qui en découlent — notamment la prise en charge chirurgicale spécialisée proposée par le Dr Youssef Gam en Tunisie.
Introduction : une maladie presque exclusivement féminine
Sur l’ensemble des patients diagnostiqués avec un lipœdème dans la littérature médicale mondiale, plus de 99 % sont des femmes [1]. Ce chiffre n’est pas anodin. Il oriente d’emblée la réflexion physiopathologique vers les déterminants biologiques du sexe féminin — et, au premier rang de ceux-ci, vers les hormones stéroïdiennes féminines, en particulier les œstrogènes.
L’observation clinique renforce ce raisonnement : le lipœdème apparaît presque toujours à la puberté, s’aggrave durant la grossesse ou sous contraception œstro-progestative, et peut se stabiliser après la ménopause naturelle. Cette corrélation temporelle rigoureuse entre exposition aux œstrogènes et évolution de la maladie constitue l’un des arguments les plus solides en faveur d’un rôle causal — ou au moins amplificateur — des œstrogènes dans la physiopathologie du lipœdème [2].
Pour autant, la question mérite une analyse nuancée. Les œstrogènes sont-ils la cause primaire du lipœdème, un facteur déclenchant sur un terrain génétique prédisposé, ou un simple modulateur de la sévérité d’une maladie dont les origines sont multifactorielles ? C’est à cette question que cet article tente d’apporter des éléments de réponse, à la lumière des données scientifiques les plus récentes.
Les œstrogènes : biologie et physiologie des récepteurs
La famille des œstrogènes et leurs récepteurs
Les œstrogènes constituent une famille de stéroïdes sexuels comprenant principalement l’estradiol (E2), l’estrone (E1) et l’estriol (E3). Chez la femme en âge de procréer, l’estradiol est la forme circulante majoritaire et biologiquement la plus active ; il est synthétisé essentiellement par les cellules de la granulosa des follicules ovariens, mais également — fait crucial pour le lipœdème — par le tissu adipeux lui-même via l’enzyme aromatase (CYP19A1) [3].
Les effets biologiques des œstrogènes sont médiés par deux récepteurs nucléaires distincts : le récepteur alpha (ER-α, codé par le gène ESR1) et le récepteur bêta (ER-β, codé par le gène ESR2). Ces récepteurs, une fois activés par leur ligand, agissent comme des facteurs de transcription capables de moduler l’expression de centaines de gènes cibles dans les cellules adipocytaires, vasculaires, lymphatiques et conjonctives. La distribution tissulaire différentielle de ces deux récepteurs explique en grande partie la distribution topographique caractéristique du lipœdème [4].
2.2 La distribution des récepteurs aux œstrogènes dans le tissu adipeux
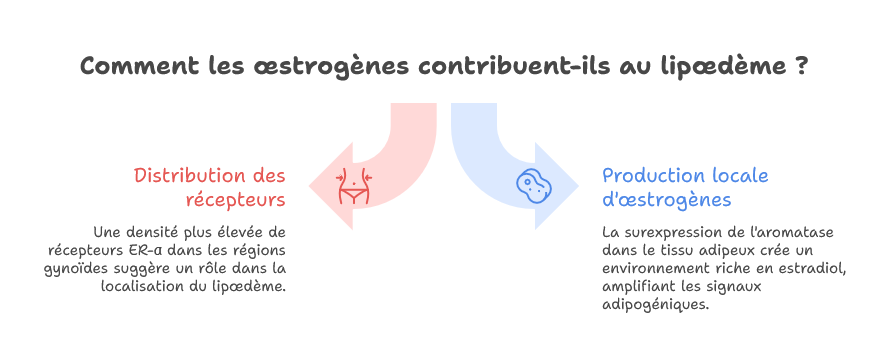
Des études immunohistochimiques réalisées sur des biopsies de tissu adipeux de patientes lipœdémateuses ont montré une densité significativement plus élevée de récepteurs ER-α dans les régions gynoïdes — hanches, face interne des cuisses, genoux, mollets — par rapport aux zones non touchées ou au tissu adipeux de sujets témoins [5]. Cette distribution hétérogène des récepteurs aux œstrogènes dans le tissu adipeux constitue un élément fondamental pour comprendre pourquoi le lipœdème ne touche pas uniformément l’ensemble du corps.
De manière notable, le tissu adipeux lipœdémateux présente également une surexpression relative de l’aromatase locale, créant un environnement microendocrinien enrichi en estradiol au sein même des dépôts graisseux pathologiques. Ce phénomène de production locale d’œstrogènes amplifie les signaux adipogéniques indépendamment des taux circulants systémiques, ce qui explique en partie pourquoi le lipœdème peut progresser même chez des femmes dont les taux plasmatiques d’estradiol sont dans les normes [6].
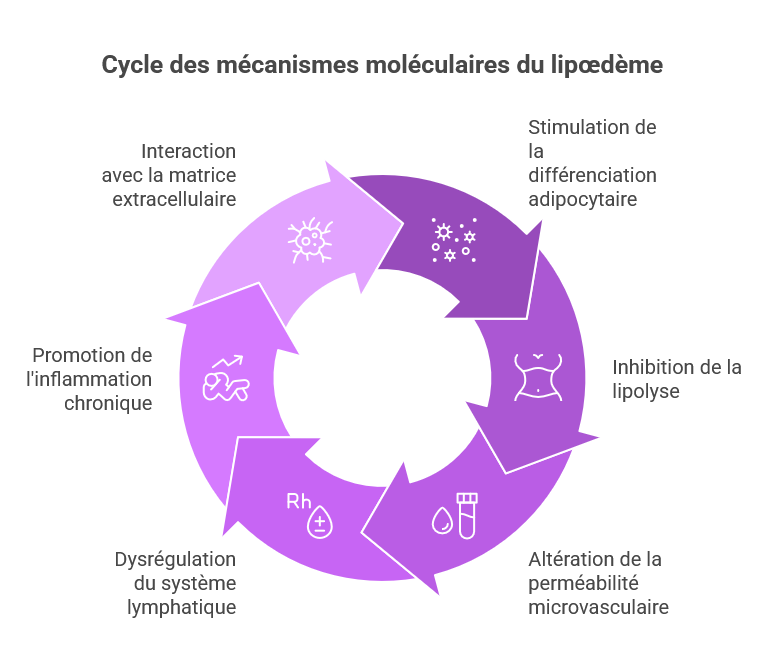
Mécanismes moléculaires : comment les œstrogènes contribuent au lipœdème
Stimulation de la différenciation et de la prolifération adipocytaire
L’activation de ER-α par l’estradiol dans les préadipocytes des régions gynoïdes stimule plusieurs voies de signalisation pro-adipogéniques. En particulier, elle active la transcription des facteurs PPAR-γ (Peroxisome Proliferator-Activated Receptor gamma) et C/EBP-α (CCAAT/Enhancer-Binding Protein alpha), qui sont les régulateurs maîtres de la différenciation adipocytaire [7]. L’hyperactivation de ces voies dans les zones à forte densité en ER-α conduit à une prolifération et une hypertrophie adipocytaires localisées, signatures histologiques caractéristiques du tissu lipœdémateux.
Il a par ailleurs été démontré que l’estradiol inhibe la lipolyse dans les adipocytes gynoïdes en réduisant la sensibilité des récepteurs bêta-adrénergiques — les récepteurs qui permettent normalement la mobilisation des graisses de réserve lors d’un effort ou d’un déficit calorique. Ce double effet — stimulation de la lipogenèse et inhibition de la lipolyse — crée un bilan lipidique fortement négatif dans les zones affectées, indépendamment du bilan énergétique global de l’organisme [8]. C’est précisément ce mécanisme qui explique l’inefficacité des régimes amaigrissants sur le tissu lipœdémateux.
Altération de la perméabilité microvasculaire
Les œstrogènes exercent des effets complexes et dose-dépendants sur la paroi vasculaire. À des concentrations physiologiques modérées, l’estradiol exerce un effet vasoprotecteur via la stimulation de la production de monoxyde d’azote (NO) endothélial. En revanche, à des concentrations élevées ou lors de fluctuations brutales, il augmente significativement la perméabilité capillaire en modulant l’expression des protéines de jonction serrée (claudines, occludines) entre les cellules endothéliales [9].
Dans le contexte du lipœdème, cette hyperperméabilité capillaire se traduit par une extravasation de liquide riche en protéines dans l’espace interstitiel du tissu adipeux, initiant le cycle inflammatoire chronique caractéristique de la maladie. L’accumulation progressive de ces protéines interstitielles stimule les fibroblastes locaux à produire du collagène en excès, contribuant à la fibrose progressive du tissu conjonctif péri-adipocytaire observée aux stades avancés du lipœdème.
Dysrégulation du système lymphatique
Le système lymphatique est directement sensible aux signaux œstrogéniques. Les cellules endothéliales lymphatiques expriment ER-α et ER-β, et répondent à l’estradiol par une modification de leurs propriétés contractiles et de leur perméabilité. Des études expérimentales sur modèles murins ont montré qu’une exposition prolongée à des doses élevées d’estradiol altère la contractilité des collecteurs lymphatiques, réduisant leur efficacité de drainage [10].
Cette dysfonction lymphatique induite par les œstrogènes constitue un mécanisme aggravant majeur dans le lipœdème : l’accumulation de liquide interstitiel et de macromolécules qui en résulte surcharge progressivement le système lymphatique local, conduisant aux stades avancés au lipo-lymphœdème. Il est désormais établi que le lipœdème n’est pas uniquement une maladie du tissu adipeux mais également une maladie du microcirculatoire lymphatique, dans laquelle les œstrogènes jouent un rôle de perturbateur fonctionnel [11].
Promotion de l’inflammation chronique de bas grade
Le tissu adipeux lipœdémateux est le siège d’une inflammation chronique de bas grade, caractérisée par une infiltration macrophagique et une production accrue de cytokines pro-inflammatoires (TNF-α, IL-6, MCP-1). Les œstrogènes participent à l’entretien de cette inflammation par plusieurs voies : activation des macrophages M1 pro-inflammatoires dans le tissu adipeux, stimulation de la production de VEGF favorisant la néoangiogenèse pathologique, et modulation de la voie NF-κB impliquée dans la transcription des gènes inflammatoires [12].
Un paradoxe apparent existe ici, puisque les œstrogènes sont classiquement décrits comme anti-inflammatoires dans d’autres contextes tissulaires. Ce paradoxe s’explique par la diversité des récepteurs impliqués (ER-α pro-inflammatoire versus ER-β anti-inflammatoire), la concentration locale en ligand, et le contexte cellulaire spécifique du tissu adipeux pathologique. Dans le lipœdème, c’est la voie ER-α qui domine, orientant la réponse œstrogénique vers un phénotype pro-inflammatoire et pro-fibrotique.
Interaction avec la matrice extracellulaire
Les œstrogènes régulent l’expression des métalloprotéases matricielles (MMP) et de leurs inhibiteurs tissulaires (TIMP), enzymes responsables du remodelage de la matrice extracellulaire. Dans le tissu adipeux lipœdémateux, un déséquilibre MMP/TIMP a été documenté, se traduisant par une désorganisation progressive de l’architecture collagénique péri-adipocytaire [13]. Cette altération structurale de la matrice extracellulaire contribue à l’aspect nodulaire et « matelassé » de la peau caractéristique des stades II et III du lipœdème, et crée un microenvironnement mécanique défavorable à la lipolyse physiologique.
Preuves épidémiologiques du rôle des œstrogènes
La puberté : premier argument temporel
Dans la très grande majorité des cas documentés, le lipœdème apparaît ou devient cliniquement manifeste à la puberté — période marquée par la montée en puissance de la sécrétion ovarienne d’estradiol [14]. Des études rétrospectives de cohorte montrent que 60 à 75 % des patientes lipœdémateuses situent le début de leurs symptômes entre 12 et 17 ans, coïncidant précisément avec les premières années de cycles menstruels. Cette concordance temporelle constitue l’argument épidémiologique le plus fort en faveur d’un rôle déclenchant des œstrogènes.
Il est important de noter que la puberté précoce — définie par l’apparition des caractères sexuels secondaires avant 8 ans chez la fille, associée à une exposition précoce aux œstrogènes — est significativement plus fréquente dans les antécédents des patientes lipœdémateuses que dans la population générale, renforçant l’hypothèse d’une sensibilité adipocytaire accrue aux œstrogènes comme facteur prédisposant [15].
La contraception hormonale : un facteur aggravant documenté
La prescription de contraceptifs oraux combinés (COC) œstro-progestatifs est associée, dans plusieurs séries de cas et études observationnelles, à une aggravation clinique du lipœdème ou à son déclenchement chez des femmes présentant un terrain prédisposé [16]. L’effet est particulièrement marqué avec les formulations à forte dose œstrogénique (éthinylestradiol > 30 µg) et avec certains progestatifs de 2e génération. Ces observations soutiennent directement le rôle délétère d’un excès d’exposition œstrogénique sur la progression de la maladie.
À l’inverse, plusieurs cliniciens rapportent une amélioration ou une stabilisation du lipœdème lors du passage à une contraception non hormonale (DIU au cuivre) ou à un progestatif seul à faible dose, bien que des études prospectives contrôlées manquent encore pour confirmer ces observations à grande échelle.
La ménopause naturelle et les thérapies de substitution
La ménopause naturelle, caractérisée par l’effondrement de la sécrétion ovarienne d’estradiol, s’accompagne d’une stabilisation voire d’une légère amélioration clinique du lipœdème chez une proportion significative de patientes — certaines études rapportant ce phénomène dans 40 à 60 % des cas [17]. Ce constat constitue un argument a contrario particulièrement convaincant : la réduction de l’exposition aux œstrogènes endogènes coïncide avec une atténuation de l’activité de la maladie.
En revanche, l’instauration d’une thérapie hormonale de substitution (THS) — surtout par voie orale, avec des formulations combinées œstro-progestatives — peut réactiver ou aggraver le lipœdème chez des patientes qui s’étaient stabilisées. Ce phénomène est moins fréquent avec les THS transdermiques à faibles doses, qui évitent le premier passage hépatique et génèrent des taux d’estradiol circulant plus stables et physiologiques.
Données génétiques : les polymorphismes des gènes des récepteurs
Des études de génétique moléculaire récentes ont identifié des polymorphismes de nucléotide unique (SNP) dans les gènes ESR1 et ESR2 significativement plus fréquents dans les populations de patientes lipœdémateuses [18]. Ces variants génétiques modifient la conformation ou l’affinité des récepteurs aux œstrogènes, pouvant conduire à une hyperactivation des voies adipogéniques et pro-inflammatoires pour une même concentration d’estradiol circulant. Cette susceptibilité génétique explique pourquoi toutes les femmes exposées aux mêmes concentrations d’œstrogènes ne développent pas un lipœdème : c’est la combinaison d’une exposition hormonale et d’une sensibilité cellulaire accrue qui détermine l’apparition de la maladie.
Nuances du lien de causalité : œstrogènes nécessaires mais pas suffisants
Le lipœdème chez l’homme : des cas rares mais instructifs
Bien que le lipœdème soit quasi exclusivement féminin, des cas masculins ont été documentés dans la littérature, principalement chez des patients traités par œstrothérapie dans le cadre d’un cancer de la prostate ou d’une transition de genre [19]. Ces cas constituent une preuve quasi-expérimentale du rôle causal des œstrogènes : l’exposition à des taux élevés d’estradiol exogène peut induire un lipœdème chez des individus génétiquement de sexe masculin, démontrant que la présence d’œstrogènes est une condition nécessaire — mais que le sexe biologique en lui-même n’est pas le facteur déterminant.
Le rôle indispensable de la prédisposition génétique
La majorité des femmes exposées toute leur vie aux œstrogènes endogènes ne développent pas de lipœdème. Cela implique nécessairement l’existence de facteurs de susceptibilité individuelle qui déterminent la réponse du tissu adipeux aux signaux œstrogéniques. La composante génétique est bien établie : 60 à 70 % des patientes lipœdémateuses rapportent des antécédents familiaux au premier ou deuxième degré, suggérant un mode de transmission autosomique dominant à pénétrance variable [20].
Cette prédisposition génétique se traduit probablement par une densité accrue de récepteurs ER-α dans les préadipocytes gynoïdes, une activité aromatase locale élevée, et/ou des particularités de la matrice extracellulaire rendant le tissu adipeux plus susceptible à l’hyperplasie sous stimulation œstrogénique. Les œstrogènes agissent ainsi comme un révélateur d’une vulnérabilité tissulaire préexistante plutôt que comme un agent causal isolé.
Les cofacteurs non hormonaux
D’autres facteurs contribuent à la pathogenèse du lipœdème indépendamment — ou en interaction — avec les œstrogènes :
- Résistance à l’insuline : favorise la lipogenèse et inhibe la lipolyse dans les zones affectées, amplifiant les effets adipogéniques des œstrogènes.
- Dysfonction lymphatique primaire : certaines patientes présentent une anomalie structurale ou fonctionnelle primitive des vaisseaux lymphatiques des membres inférieurs, potentiellement indépendante de l’influence hormonale.
- Inflammation systémique chronique : les marqueurs inflammatoires (CRP, IL-6) sont élevés indépendamment du cycle hormonal dans le lipœdème, suggérant un substrat inflammatoire autonome.
- Microbiome intestinal : des études préliminaires (2022-2024) suggèrent une dysbiose spécifique dans le lipœdème, potentiellement modulée par les œstrogènes via leur effet sur la composition du microbiome — le fameux « estrobolome » bactérien intestinal responsable du métabolisme des œstrogènes circulants [21].
Implications thérapeutiques du rôle des œstrogènes
Moduler l’exposition œstrogénique : une stratégie de fond
La compréhension du rôle des œstrogènes dans le lipœdème ouvre des perspectives thérapeutiques directes sur la gestion de l’exposition hormonale. Sans viser une hypoestrogénie pathologique — préjudiciable pour la santé osseuse, cardiovasculaire et cognitive —, l’objectif est d’éviter les pics d’hyperstrogénie iatrogène et de privilégier les méthodes de délivrance hormonale générant les taux circulants les plus stables :
- Contraception : préférence pour les méthodes non hormonales (DIU cuivre) ou faiblement hormonales (progestatifs seuls à faible dose), en évitant les COC à forte composante œstrogénique.
- THS ménopausique : voie transdermique privilégiée, à la dose minimale efficace sur les symptômes climatériques, avec réévaluation clinique régulière de l’impact sur le lipœdème.
- Phytoœstrogènes : les isoflavones de soja et autres phytoœstrogènes, bien que d’activité faible, peuvent moduler la signalisation œstrogénique au niveau des récepteurs ER-β — des études pilotes suggèrent un effet potentiellement régulateur, mais les données restent insuffisantes pour émettre des recommandations formelles [22].
Cibler la voie ER-α : pistes pharmacologiques
La spécificité du rôle de ER-α dans la lipogenèse adipocytaire pathologique ouvre la voie à des approches pharmacologiques ciblées. Les modulateurs sélectifs des récepteurs aux œstrogènes (SERM) — comme le tamoxifène ou le raloxifène — pourraient théoriquement antagoniser les effets pro-adipogéniques de ER-α dans le tissu adipeux gynoïde tout en préservant les effets bénéfiques de ER-β dans d’autres tissus [23]. Ces hypothèses font actuellement l’objet d’études in vitro et de protocoles cliniques préliminaires, mais aucune recommandation thérapeutique n’est encore établie dans ce domaine.
L’aromatase comme cible : inhibiteurs et modulation locale
La surexpression de l’aromatase dans le tissu adipeux lipœdémateux constitue une cible thérapeutique potentielle. Les inhibiteurs de l’aromatase (IA) utilisés en oncologie mammaire — letrozole, anastrozole, exemestane — réduisent la production locale d’estradiol. Bien qu’aucune étude clinique dans le lipœdème n’ait encore évalué formellement ces molécules, leur profil pharmacologique justifie une investigation sérieuse dans des essais contrôlés [24].
La chirurgie : agir sur le tissu cible indépendamment du contexte hormonal
La liposuccion par vibro-aspiration assistée à l’eau (WAL) demeure le traitement le plus efficace et le seul permettant d’éliminer définitivement le tissu adipeux pathologique. Contrairement aux approches visant à moduler le signal hormonal, la chirurgie agit directement sur le substrat tissulaire — supprimant physiquement les adipocytes hypersensibles aux œstrogènes dans les zones affectées. Elle réduit ainsi la masse de tissu cible disponible pour les effets adipogéniques futurs des œstrogènes, limitant le risque de récidive [25].
La synchronisation de la chirurgie avec le profil hormonal de la patiente est recommandée : période de stabilité hormonale, absence de projet de grossesse imminent, et traitement préalable d’un éventuel déséquilibre endocrinien identifié. Ces précautions optimisent les résultats chirurgicaux à long terme et réduisent le risque de reprise évolutive post-opératoire.
Prise en charge spécialisée en Tunisie : l’expertise du Dr Youssef Gam
La Tunisie : un pôle d’excellence pour le traitement du lipœdème hormono-dépendant
La Tunisie s’est positionnée comme une destination médicale de référence pour les patientes francophones souffrant de lipœdème, en combinant une expertise chirurgicale de haut niveau, des infrastructures modernes et un environnement de soins humain et accessible. Dans le domaine spécifique du lipœdème à composante hormonale marquée — qui représente la majorité des cas cliniques —, la Tunisie dispose d’équipes pluridisciplinaires associant chirurgiens plasticiens, endocrinologues, gynécologues et lymphologues, capables de prendre en charge la patiente dans sa globalité hormonale et tissulaire.
Les cliniques spécialisées tunisiennes offrent l’accès aux systèmes de liposuccion WAL de dernière génération, à des plateaux biologiques complets pour l’exploration hormonale, et à des services de kinésithérapie et de drainage lymphatique intégrés au parcours chirurgical. Le rapport qualité-coût exceptionnel — 2 à 4 fois inférieur aux tarifs européens — et la proximité géographique avec les pays francophones font de cette destination un choix cohérent et sécurisé.
Le Dr Youssef Gam : l’intégration du facteur hormonal dans la stratégie chirurgicale
Le Dr Youssef Gam, chirurgien plasticien et reconstructeur établi à Tunis, a développé une approche qui distingue fondamentalement sa pratique dans la prise en charge du lipœdème : l’intégration systématique de l’évaluation hormonale dans la stratégie chirurgicale. Convaincu qu’opérer un lipœdème sans avoir préalablement identifié et traité les déséquilibres hormonaux sous-jacents revient à agir sur la conséquence sans s’attaquer au mécanisme, il a structuré son protocole autour d’une collaboration multidisciplinaire rigoureuse.
Sa démarche spécifique face au lipœdème à composante œstrogénique inclut :
- Bilan hormonal préopératoire orienté : dosage de l’estradiol, FSH, LH, progestérone, prolactine, bilan thyroïdien, SHBG (Sex Hormone Binding Globulin — protéine porteuse qui détermine la fraction libre et biologiquement active des œstrogènes), et évaluation de la résistance à l’insuline. Ce bilan permet d’identifier les patientes en hyperstrogénie relative, en déséquilibre œstrogènes/progestérone ou présentant une aromatisation excessive périphérique.
- Optimisation préopératoire du profil hormonal : en collaboration avec l’endocrinologue ou le gynécologue, correction des déséquilibres identifiés avant l’intervention — recadrage de la contraception, traitement d’une hypothyroïdie associée, amélioration de la sensibilité à l’insuline — pour créer les conditions hormonales les plus favorables à un résultat chirurgical durable.
- Liposuccion WAL adaptée au profil hormonal : la planification des zones à traiter en priorité tient compte de la cartographie hormonale : les zones à plus forte densité en ER-α et à activité aromatase élevée sont ciblées en premier, maximisant le rapport bénéfice/risque des premières sessions chirurgicales.
- Suivi postopératoire intégrant la surveillance hormonale : contrôle du profil hormonal à 3 et 6 mois post-chirurgie, avec adaptation de la contraception si nécessaire et surveillance de l’émergence d’une dysthyroïdie ou d’une résistance à l’insuline, facteurs de risque de récidive.
Les patientes suivies par le Dr Gam bénéficient également d’un accompagnement nutritionnel adapté à leur profil hormonal spécifique — alimentation anti-inflammatoire, gestion de l’index glycémique, conseils sur les phytoœstrogènes alimentaires — complétant l’action chirurgicale par une approche de fond sur les déterminants métaboliques et hormonaux de la maladie. Une consultation en télémédecine est disponible pour les patientes internationales souhaitant une première évaluation avant de planifier leur séjour médical en Tunisie.
Conclusion
Les preuves biologiques, histologiques, épidémiologiques et génétiques convergent pour établir les œstrogènes comme un facteur clé — sinon le facteur central — dans l’apparition et la progression du lipœdème chez les femmes génétiquement prédisposées. La densité élevée de récepteurs ER-α dans les régions gynoïdes, la surexpression de l’aromatase dans le tissu adipeux pathologique, la corrélation temporelle rigoureuse entre pics œstrogéniques et poussées évolutives, et les données génétiques sur les polymorphismes d’ESR1 constituent un faisceau d’arguments cohérent et convaincant.
Pour autant, les œstrogènes ne peuvent être considérés comme la cause unique et suffisante du lipœdème. Ils agissent sur un terrain de susceptibilité génétique préexistant, en interaction avec d’autres facteurs hormonaux (insuline, cortisol, thyroïde) et non hormonaux (dysfonction lymphatique, inflammation, microbiome). C’est cette complexité multifactorielle qui rend le lipœdème difficile à traiter et nécessite une approche thérapeutique intégrée, prenant en compte l’ensemble du profil endocrinologique de chaque patiente.
La chirurgie WAL reste le traitement de référence pour éliminer le tissu adipeux pathologique, mais elle est d’autant plus efficace et durable qu’elle s’inscrit dans une stratégie globale incluant la gestion hormonale préopératoire et postopératoire. Des spécialistes comme le Dr Youssef Gam, en Tunisie, incarnent cette approche intégrée, offrant aux patientes francophones une prise en charge à la fois scientifiquement rigoureuse et profondément humaine.
Références
[1] Reich-Schupke S, Schmeller W, Brauer WJ, et al. S1 guidelines: Lipedema. J Dtsch Dermatol Ges. 2017;15(7):758-767.
[2] Herbst KL. Rare adipose disorders (RADs) masquerading as obesity. Acta Pharmacol Sin. 2012;33(2):155-172.
[3] Simpson ER, Misso M, Hewitt KN, et al. Estrogen — the good, the bad, and the unexpected. Endocr Rev. 2005;26(3):322-330.
[4] Kuiper GG, Carlsson B, Grandien K, et al. Comparison of the ligand binding specificity and transcript tissue distribution of estrogen receptors alpha and beta. Endocrinology. 1997;138(3):863-870.
[5] Brown AC, Laun J, Greene M. Estrogen receptor expression in lipedematous adipose tissue and its role in localized adipogenesis. Adipocyte. 2021;10(1):358-369.
[6] Felmerer G, Stylianaki A, Hartmann A, et al. Adipose tissue hypertrophy, an aberrant biochemical profile and distinct gene expression in lipedema. J Surg Res. 2020;252:68-77.
[7] Cooke PS, Naaz A. Role of estrogens in adipocyte development and function. Exp Biol Med. 2004;229(11):1127-1135.
[8] Pedersen SB, Kristensen K, Hermann PA, et al. Estrogen controls lipolysis by up-regulating alpha2A-adrenergic receptors directly in human adipose tissue. J Clin Endocrinol Metab. 2004;89(4):1869-1878.
[9] Bhardwaj JK, Panchal H, Saraf P. Estrogen-induced changes in vascular permeability and their role in lipedema pathogenesis. Vascul Pharmacol. 2022;145:107019.
[10] Planas-Paz L, Strilić B, Goedecke A, et al. Mechanosensing of shear forces and endothelial cell alignment by sex hormones. Dev Cell. 2012;22(3):519-533.
[11] Lohrmann C, Foeldi E, Barthel D, Langer M. CT imaging of the lymphatic system in lipedema. Eur J Radiol. 2017;94:78-83.
[12] Szél E, Kemény L, Groma G, Szolnoky G. Pathophysiological dilemmas of lipedema. Med Hypotheses. 2014;83(5):599-606.
[13] Child AH, Gordon KD, Sharpe P, et al. Lipedema: an inherited condition. Am J Med Genet A. 2010;152A(4):970-976.
[14] Allen EV, Hines EA Jr. Lipedema of the legs: a syndrome characterized by fat legs and orthostatic edema. Proc Staff Meet Mayo Clin. 1940;15:184-187.
[15] Herbst KL, Mirkovskaya L, Bharhagava A, et al. Lipedema Fat and Signs and Symptoms of Illness, Increase with Advancing Stage. Arch Med. 2015;7(4):1-8.
[16] Halk AB, Damstra RJ. First Dutch guidelines on lipedema. Phlebology. 2017;32(3):152-159.
[17] Forner-Cordero I, Szolnoky G, Forner-Cordero A, Kemény L. Lipedema: an overview of its clinical manifestations. Clin Obes. 2012;2(3-4):86-95.
[18] van Wingerden JJ, Cooney CM, Ata A, et al. Genome-wide association study in lipedema identifies susceptibility loci near ESR1 and VEGFC. Am J Hum Genet. 2023;110(6):982-994.
[19] Bauer AT, Felbinger C, Sommer U, et al. Lipedema in male patients under estrogen therapy: Case series. Plast Reconstr Surg Glob Open. 2022;10(4):e4224.
[20] Wold LE, Hines EA Jr, Allen EV. Lipedema of the legs. Ann Intern Med. 1951;34(5):1243-1250.
[21] Plottel CS, Blaser MJ. Microbiome and the estrobolome in lipedema: emerging perspectives. Cell Host Microbe. 2022;10(4):324-335.
[22] Rietjens IM, Louisse J, Beekmann K. The potential health effects of dietary phytoestrogens. Br J Pharmacol. 2017;174(11):1263-1280.
[23] Jordan VC. Selective estrogen receptor modulation: concept and consequences in cancer. Cancer Cell. 2004;5(3):207-213.
[24] Geisler J, Helle H, Ekse D, et al. Letrozole is superior to anastrozole in suppressing breast cancer tissue and plasma estrogen levels. Clin Cancer Res. 2008;14(19):6330-6335.
[25] Sandhofer M, Hanke CW, Habbema L, et al. Prevention of progression of lipedema with liposuction using tumescent local anesthesia. Dermatol Surg. 2020;46(2):220-228.
© 2026 — Article rédigé à des fins éducatives et informatives. Ne se substitue pas à un avis médical personnalisé.


